Eine 100-prozentige Verifizierungsrate durch Point-of-Interest-IR-Spektroskopie
Optische Sensoren in der Qualitätssicherung und Prozesskontrolle
Qualität sichern ohne Zeit zu verlieren: Besonders Unternehmen aus der Pharma-, Chemie- und Lebensmittelbranche sind darauf angewiesen, höchste Qualitätsanforderungen zu erfüllen und zugleich Produktionsprozesse zu optimieren. Das Fraunhofer IAF hat für solche Prozesse ein integrierbares Messsystem entwickelt, das mit Hilfe von maschinellem Sehen gezielt Proben erkennt und innerhalb von wenigen Millisekunden mittels laser-basierter Mittelinfrarot-Spektroskopie kontaktfrei verifiziert.
Mit einem inline-fähigen, laserbasierten Infrarotspektroskopie-Messsystem möchten Forschende des Fraunhofer-Instituts für Angewandte Festkörperphysik (IAF) Industrieunternehmen aus der Pharma-, Chemie- und Lebensmittelbranche dabei unterstützen, Maßnahmen zur Qualitätssicherung sowie Prozesskontrollen zuverlässiger und zugleich effizienter zu gestalten.
Das Verifizierungsprinzip des entwickelten und am IAF in Freiburg ausgestellten Technologie-Demonstrators basiert auf der Point-of-Interest-Spektroskopie (POI): Ein spektral-breitbandiger mittelinfraroter (IR) Laserstrahl wird selektiv auf relevante, zu vermessene Positionen gelenkt, das diffus reflektierte Rückstreuspektrum wird aufgenommen und in Echtzeit ausgewertet. Pro Probe können eine oder mehrere Messstellen definiert werden, sodass der Anwender schnell Informationen über Qualität und Homogenität einer laufenden Probenreihe beziehungsweise eines Produktions-Batches bekommen kann. Die Messung pro Messstelle dauert je nach zeitlicher Mittelung zwischen einer und 20 Millisekunden. Sie erfolgt kontaktlos und ist durch den geringen Energieertrag vom IR-Licht zerstörungsfrei.
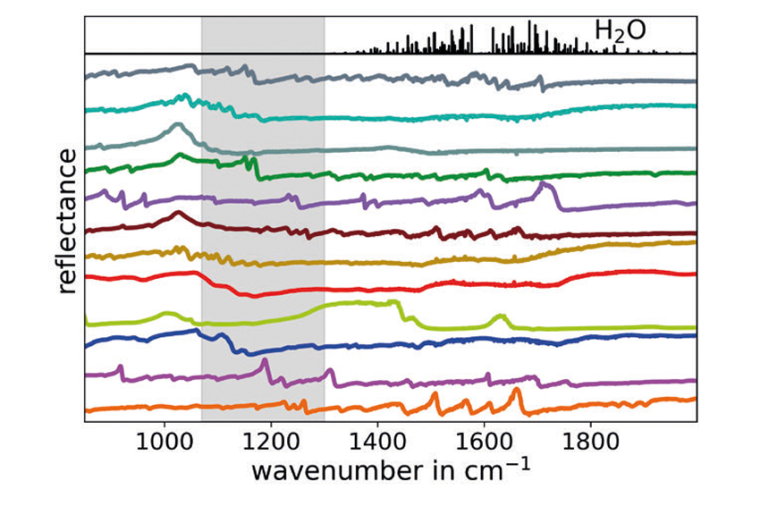
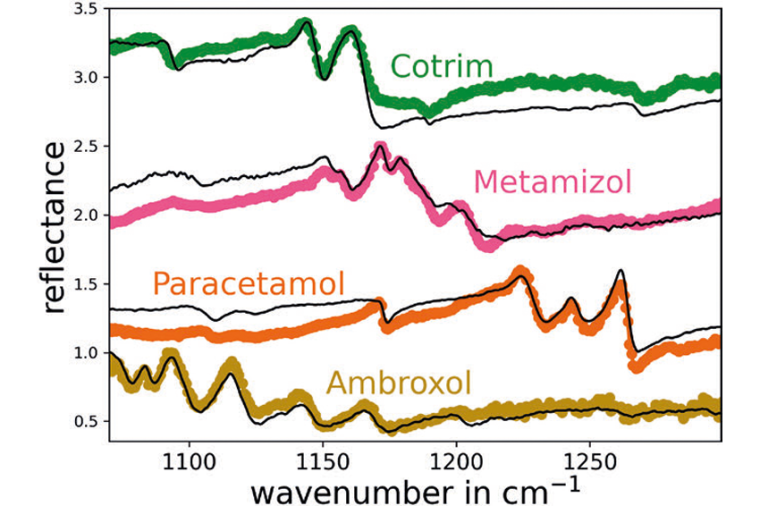
Die bei der Messung gewonnenen Informationen basieren auf der Wechselwirkung der Probe mit dem gelenkten IR-Laserstrahl – in diesem Fall ein Frequenz-abstimmbarer Quantenkaskadenlaser (QCL). Je nach chemischer Zusammensetzung der Probe, sowie derer Oberflächenmorphologie, nimmt das System die charakteristischen IR-Rückstreuspektren auf und zieht Rückschlüsse auf die Probenqualität. Durch die Verwendung von IR-Spektralbanden (im Gegensatz zu nah-infraroten (NIR) Spektralbanden, die funktionelle Gruppen sowie Obertöne adressieren) lässt sich eine hohe Selektivität zwischen den erprobten Substanzen erreichen, was die Zuverlässigkeit in der Qualitätskontrolle signifikant erhöht. Weitere Bereiche des zur Identifizierung relevanten Infrarotbereiches weisen eine sehr gute Transmission auf, was Stand-Off-Messungen ermöglicht.

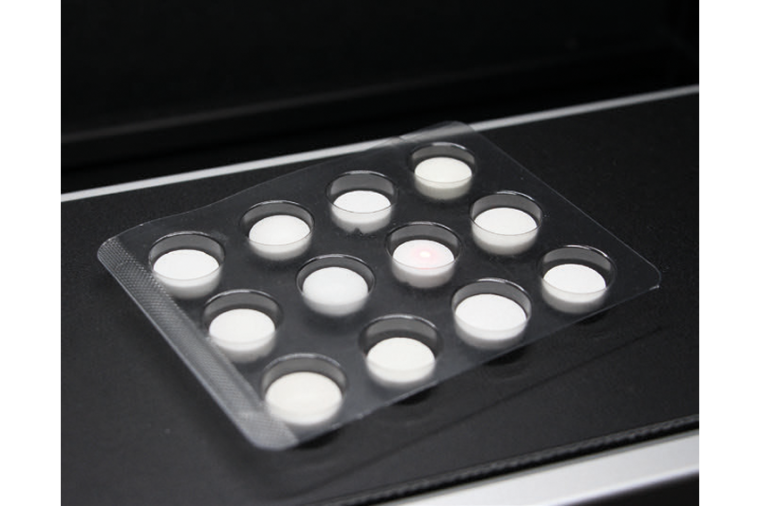

Je nach Systemauslegung sind Messabstände zwischen einigen Zentimetern und mehreren Metern realisierbar. Der Technologie-Demonstrator hat einen Messabstand von 30 cm und ist darauf ausgelegt, die Anwendbarkeit des Messprinzips der POI-Spektroskopie für die Inline-Qualitätskontrolle bei der Produktion von pharmazeutischen Blistern zu illustrieren [1].
Verifizierung von Blister-Inhalten mittels POI-IR-Spektroskopie
Die Herstellung von pharmazeutischen Produkten unterliegen verschiedensten Normen und (EU-) Richtlinien. Die Qualitätssicherung ist daher von herausragender Bedeutung und wird unter dem Stichwort GMP (Good Manufacturing Practice) zusammengefasst [2]. Herausfordernd sind hierbei Prozesse, in denen Produkte vermischt werden können, wie bei der Verblisterung von identisch aussehenden, aber unterschiedlichen Produkten auf einer Verpackungslinie oder bei der patientenspezifischen Verblisterung. Hierbei kommen heute oft Inspektionssysteme zum Einsatz, die im sichtbaren Spektralbereich arbeiten, die jedoch keine Informationen über die Zusammensetzung der Tabletten liefern. Die POI-IR-Spektroskopie ist hier eine sinnvolle Ergänzung.
Das entwickelte Blister-Verifizierungs-System besteht aus den folgenden Hauptkomponenten:
- Sichtbare Kamera (VIS), die einen durch die Systemauslegung definierten Bereich (etwa 15 x 15 cm) des Förderbands überwacht. Dieser Bereich wird im folgenden Region-of-Interest (ROI) genannt.
- Förderband, das Proben (beziehungsweise Blister mit einer beliebigen Anzahl von Pillen und Pillenkombinationen enthält) in die ROI transportiert.
- IR-Lichtquelle: Frequenz-abstimmbarer MOEMS EC-QCL (Mikro-Opto-Elektro-Mechanisches-System External-Cavity-Quantenkaskadenlaser) mit Steuerungselektronik.
- Strahlführungssystem, mit welchem der ROI Bereich durch gezielte Lenkung des QCL-Strahls durchgerastert werden kann.
- Optiksystem zum Einsammeln des diffusen IR-Rückstreulichtes. Dieses wird anschließend auf einen schnellen und IR-Detektor fokussiert.
Sobald ein Blister in der ROI eingetroffen ist, stoppt das Förderband automatisch. Mit maschinellem Sehen werden die Pixel-Koordinaten der POIs aus dem Kamerabild des Blisters ermittelt. Diese Koordinaten werden dann auf Basis einer vorher durchgeführten Kalibrierung in 2D-Spannungs-Koordinaten übersetzt, sodass der IR-Laser und die kollineare Empfangsoptik mit dem verwendeten 2D-Galvo auf die gewünschte Pixelposition gelenkt werden kann. Anschließend wird der spektrale Scan durchgeführt.
IR-Spektroskopie mit Kilohertzraten
Herzstück des gesamten Systems ist der MOEMS-EC-QCL, welcher die IR-Spektroskopie mit Kilohertzraten ermöglicht. Ein MOEMS-basiertes Beugungsgitter ist mit dem breitbandig-emittierenden QCL-Chip in einem kompakten Modul in einer optischen External-Cavity-Konfiguration verbaut [3]. Das Abstimmen der Emissionswellenlänge erfolgt durch das mikromechanische Auslenken des MOEMS-Gitters im externen Resonator des Lasers, welches sich mit einer Frequenz von ~1 kHz (entsprechend seiner mechanischen Resonanzfrequenz) um seine Gleichgewichtslage um maximal ±10˚ oszilliert.
Über eine dedizierte Elektronik wird die MOEMS-Bewegung gesteuert und phasensynchron ein Pulszug für den im Lasermodul integrierten Lasertreiber zum Beginn jeder neuen MOEMS-Oszillation erzeugt. Dieser ist auf die Dauer einer MOEMS-Periode beschränkt. Typischerweise wird der QCL mit einem Tastgrad von 5 bis 10 Prozent betrieben (Puls-Wiederholungsraten von 0,5 bis 1 MHz und Pulslängen von 0,1 μs), was in etwa 500 bis 1.000 spektralen Messpunkten pro MOEMS-Periode (Hin- und Rücklauf) resultiert. Der typische spektrale Abstimmbereich eines MOEMS-EC-QCLs beträgt ~300 cm-1, sodass spektrale Scanraten von ~300.000 cm-1s-1 erreicht werden. Diese Scangeschwindigkeit lässt sich ferner linear mit der Anzahl der verwendeten MOEMS EC-QCLs hochskalieren, indem man mehrere MOEMS EC-QCLs miteinander kombiniert, ohne dabei Messzeit oder spektrale Auflösung zu verlieren [4].
Die spektrale Auflösung ist durch die Anzahl von Messpunkten und die Linienbreite gegeben, und beträgt bei den typischen Betriebsbedingungen ~1,5 cm-1. Im Gegensatz zum Interferometer-Arm-basierten Spektrometern, zum Beispiel einem FTIR-Spektrometer, ist die erreichte spektrale Auflösung unabhängig von der Messzeit. Eine zeitliche Mittelung in einem MOEMS-EC-QCL-basierten Spektrometer führt zu einem höheren Signal-zu-Rauschen-Verhältnis. Integrationszeiten von bis zu ~10 s (~104 MOEMS-Perioden) sind typischerweise frei von langsamen Systemdrifts [3].
Spektroskopie kombiniert mit künstlicher Intelligenz
Die Auswertung der innerhalb von 0,3 s (für einen Blister mit zwölf Tabletten) aufgenommenen Spektren erfolgt anhand eines vorher trainierten künstlichen neuronalen Netzes. Ziel der Auswertung ist die möglichst genaue Klassifizierung der Tabletten (was Verwechselungsrisiken senkt). Eine nahezu 100-prozentige Genauigkeit wird für die typischen Messbedingungen (20 ms Messzeit pro Tablette, 0,3 s Messzeit pro Blister) erreicht.
Es sind jedoch auch andere Auswerteziele möglich jenseits der reinen Spektrenklassifizierung. Beispielsweise ließen sich Kontaminationsgefahr einer bestimmten Substanz oder die Verwechselungsgefahr zwischen zwei bestimmten Substanzen senken. Die Datenbearbeitung mittels maschinellen Lernens ermöglicht es, zielgerichtete beziehungsweise anwendungsspezifische Auswertealgorithmen aufzustellen.
Literatur
[1] Y. V. Flores et al., “Point of Interest Mid-Infrared Spectroscopy for Inline Pharmaceutical Packaging Quality Control,” IEEE Sensors Journal, vol. 23, no. 14, pp. 16115-16121, 2023.
[2] European Commission Directive 91/356/EEC, Health and Consumers Directorate-General, “The Rules Governing Medicinal Products in the European Union”, vol. 4 (“EU Guidelines for Good Manufacturing Practice for Medicinal Products for Human and Veterinary Use”). Februar 2011.
[3] L. Butschek et al., “Microoptoelectromechanical systems-based external cavity quantum cascade lasers for real-time spectroscopy,” Optical Engineering, vol. 57, no., 1, pp. 1-10, 2017.
[4] Y. V. Flores et al., “Phase-locked and phase-tuned resonant-MOEMS external cavity QCLs and their application for fast and broadband mid-infrared reflectometry,” CLEO-Europe Conference, München, 2023.
Autoren
Dr. Yuri V. Flores, Wissenschaftler in der Abteilung Optoelektronik des Fraunhofer IAF
Dr. Marko Härtelt, Gruppenleiter Laser-Messtechnik in der Abteilung Optoelektronik des Fraunhofer IAF
Anbieter
Fraunhofer-Institut für Angewandte Festkörperphysik IAFTullastraße 72
79108 Freiburg
Deutschland
Meist gelesen

Auf der Suche nach einer Germanium-Alternative für die LWIR-Bildgebung
Silwir bietet eine leistungsstarke Alternative zu knappem Germanium: Schutzfenster aus Silizium mit DLC- und BBAR-Beschichtungen bieten hohe Transmission und Robustheit. Mike Giznik von Midopt erklärt die Vorteile.

„Alles wird kleiner und erhält mehr Intelligenz“
Die Intralogistik gewinnt für Baumer immer mehr an Bedeutung. Über aktuelle Trends sprechen wir mit Peter Jürgen Tittes.

Was Anwender und Hersteller über den Cyber Resilience Act wissen müssen
Sicherheitsexperte Thomas Hopfner vom Softwarehersteller MVTec erklärt, warum vernetzte Produktionsumgebungen ein bevorzugtes Ziel für Angriffe sind.

Präzise bis auf den Nanometer genau
Die Interferometrie ist in der Halbleiter-, Verpackungs- und Medizinindustrie von Bedeutung. Neue Weißlichtsysteme bieten Präzision im Nanometerbereich, hohe Messraten und sind ideal für den industriellen Einsatz.

Die Zukunft der Intralogistik
Die Intralogistik befindet sich im Wandel: Der Bedarf an qualifizierten Fachkräften steigt, während gleichzeitig neue Konzepte und Technologien entstehen.







